Así es la inyección regenerativa que podría proteger el cerebro tras un ictus
Cuando ocurre, la prioridad médica es restablecer cuanto antes el flujo sanguíneo al cerebro para evitar la muerte del paciente

Fact checked
Este artículo de OkSalud ha sido verificado para garantizar la mayor precisión y veracidad posible: se incluyen, en su mayoría, estudios médicos, enlaces a medios acreditados en la temática y se menciona a instituciones académicas de investigación. Todo el contenido de OkSalud está revisado pero, si consideras que es dudoso, inexacto u obsoleto, puedes contactarnos para poder realizar las posibles modificaciones pertinentes.
Un equipo de investigadores de la Universidad Northwestern, en Estados Unidos, ha creado un nanomaterial inyectable con capacidad regenerativa que podría proteger el cerebro tras un ictus isquémico, la forma más frecuente de este accidente cerebrovascular.
Cuando ocurre un ictus, la prioridad médica es restablecer cuanto antes el flujo sanguíneo al cerebro para evitar la muerte del paciente. Sin embargo, esa misma reperfusión —aunque vital— puede desencadenar un daño secundario importante: muerte neuronal, inflamación intensa y un mayor riesgo de secuelas neurológicas permanentes.
Según un estudio preclínico reciente, los científicos administraron una sola dosis intravenosa del nuevo tratamiento justo después de restablecer la circulación sanguínea en un modelo murino de ictus isquémico. El material logró atravesar la barrera hematoencefálica, uno de los mayores obstáculos en neurología, y alcanzó directamente el tejido cerebral dañado. Como resultado, se observó una reducción significativa de la lesión cerebral sin efectos tóxicos ni daños en otros órganos.
Los hallazgos, publicados el 7 de enero en la revista Neurotherapeutics, apuntan a que esta terapia podría convertirse en el futuro en un complemento a los tratamientos actuales, ayudando a limitar el daño cerebral secundario y favoreciendo la recuperación neurológica.
«Las estrategias clínicas actuales se centran casi exclusivamente en reabrir el vaso sanguíneo», explica el doctor Ayush Batra, autor corresponsal del estudio y profesor asociado de neurología y patología en la Facultad de Medicina Feinberg de Northwestern. «Cualquier intervención capaz de proteger las neuronas y reducir el daño posterior tendría un enorme valor clínico. Aún no disponemos de ese ‘santo grial’, pero este trabajo nos acerca a él».
Moléculas dinámicas con potencial regenerativo
La terapia se basa en una plataforma de péptidos terapéuticos supramoleculares (STP), desarrollada por el científico Samuel I. Stupp, también de Northwestern. Esta tecnología, conocida como «moléculas danzantes», ya había demostrado su potencial en un estudio publicado en Science en 2021, donde logró revertir la parálisis y reparar tejido en ratones con lesiones graves de médula espinal mediante una sola inyección local.
El nuevo trabajo demuestra que ensamblajes moleculares similares pueden administrarse por vía intravenosa, sin necesidad de cirugía ni de inyecciones directas en el cerebro, lo que supone un avance clave para su posible aplicación clínica.
«Lo más prometedor es que una tecnología que ya mostró resultados extraordinarios en lesiones de la médula espinal ahora puede adaptarse al ictus y administrarse de forma sistémica», señala Stupp, profesor de Ciencia e Ingeniería de Materiales, Química, Medicina e Ingeniería Biomédica. «La capacidad de atravesar la barrera hematoencefálica abre además la puerta a su uso en traumatismos craneoencefálicos y enfermedades neurodegenerativas como la ELA».
Un modelo que replica el tratamiento real del ictus
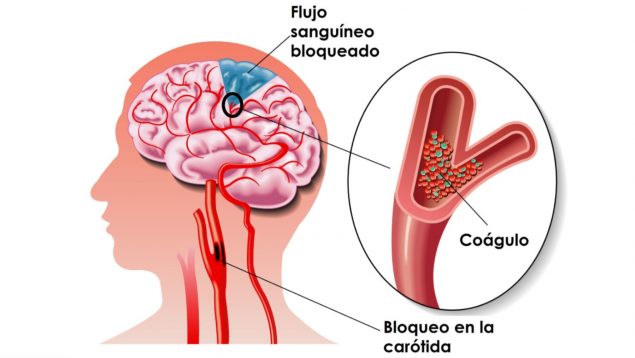
El ictus isquémico agudo representa alrededor del 80 % de los casos y es una de las principales causas de discapacidad y mortalidad a nivel mundial. Se produce cuando un coágulo bloquea el flujo sanguíneo al cerebro, y el tratamiento consiste en disolverlo con fármacos o retirarlo mediante procedimientos mecánicos.
En este estudio, los investigadores reprodujeron fielmente ese proceso: primero bloquearon el flujo sanguíneo para simular un ictus grave y después lo restablecieron, tal como ocurre en la práctica clínica. Tras el tratamiento, los ratones fueron monitorizados durante una semana sin que se detectaran problemas de toxicidad, rechazo inmunológico ni efectos adversos relevantes.
Gracias a técnicas avanzadas de imagen en tiempo real, los científicos confirmaron que el nanomaterial se acumulaba específicamente en la zona lesionada. En comparación con los animales no tratados, los que recibieron las «moléculas danzantes» presentaron menos daño cerebral, menor inflamación y una respuesta inmunitaria más controlada.
Según Stupp, el éxito de la terapia se debe a su doble acción: antiinflamatoria y proregenerativa. «Cuando se elimina el coágulo, muchas moléculas dañinas se liberan de golpe y agravan la lesión. Nuestras moléculas ayudan a neutralizar esa respuesta inflamatoria y, al mismo tiempo, favorecen la reparación de las redes neuronales», explica.
Hacia una recuperación funcional más completa
El tratamiento actúa enviando señales que estimulan la plasticidad neuronal, es decir, la capacidad del cerebro para reorganizarse y reconstruir conexiones. Entre otros efectos, puede promover el crecimiento de los axones y la reconexión entre neuronas, restaurando la comunicación perdida tras el ictus.
Batra subraya que aún serán necesarios estudios más prolongados para determinar si esta protección inicial se traduce en una mejora funcional a largo plazo, especialmente en áreas como la cognición, que suele verse afectada durante meses o incluso años después de un ictus.
Temas:
- Ictus
- Tratamientos









