Ácido nítrico: características, usos industriales y peligros
Ácido nítrico: características, usos en fertilizantes, explosivos y procesos industriales clave.
Ácido sulfúrico
¿Qué es la lluvia ácida?
Ácido que triunfa para la piel

Hay compuestos químicos que pasan desapercibidos, pero se sostienen en el medio mundo industrial. El ácido nítrico es uno de ellos. No suele aparecer en conversaciones cotidianas, pero está detrás de cosas muy concretas: fertilizantes que aumentan la producción agrícola, explosivos utilizados en minería o infraestructuras, tratamientos de metales… incluso algunos procesos electrónicos bastante precisos.
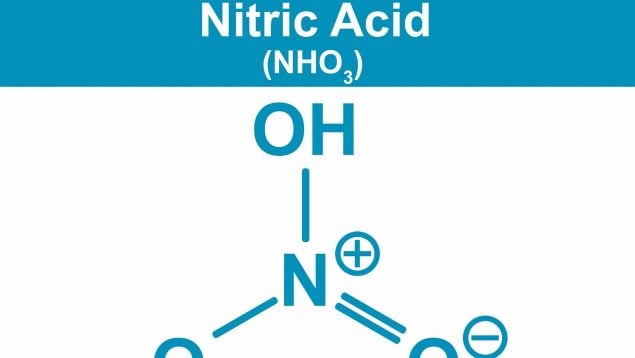
Su fórmula es HNO₃, sí. Pero quedarse ahí es como definir un coche solo por tener cuatro ruedas. Lo interesante es cómo se comporta y por qué sigue siendo tan importante hoy. Una sustancia aparentemente simple… pero intensa.
Si alguien viera ácido nítrico puro en un laboratorio, probablemente pensaría que es agua. Es transparente, líquido, sin nada llamativo, especialmente a simple vista. Ahora bien, eso dura poco. Con el paso del tiempo, o si no se almacena en condiciones adecuadas, empieza a cambiar de color. Se vuelve amarillento. ¿El motivo? Se descompone ligeramente y libera dióxido de nitrógeno, un gas marrón que acaba disolviéndose en el propio ácido.
Y luego está el olor. Fuerte, bastante penetrante. No es de esos que ignoras sin darte cuenta. A nivel químico, es un ácido fuerte. Muy fuerte. En agua se disocia casi por completo, liberando protones sin demasiada resistencia. Pero lo que realmente marca la diferencia es su carácter oxidante. No solo reacciona: transforma.
Propiedades que explican todo lo demás
Cuando se intenta entender por qué el ácido nítrico tiene tantos usos, hay que fijarse en tres o cuatro ideas clave. La primera es su agresividad química. Es corrosivo. Puede atacar metales, tejidos orgánicos, plásticos… lo que se le ponga delante, dependiendo de la concentración. No es un producto con el que se debe experimentar sin conocimiento. La segunda es su capacidad oxidante.
Luego está su facilidad para mezclarse con agua. No hay límites en ese sentido. Eso permite trabajar con distintas concentraciones según lo que se necesite, algo muy práctico en entornos industriales. Y hay un pequeño detalle que suele mencionarse en laboratorio: cuando entra en contacto con proteínas, puede teñirlas de amarillo. Es la famosa reacción xantoproteica. No tiene mucha aplicación práctica fuera de ese contexto, pero ilustra bien cómo interactúa con la materia orgánica.
De dónde sale: así se fabrica
La mayor parte del ácido nítrico que se utiliza hoy se produce mediante el proceso Ostwald. Lleva tiempo en uso, pero sigue siendo la base. Todo empieza con amoníaco. A partir de ahí, se produce una oxidación en presencia de un catalizador, normalmente platin, y se obtiene óxido nítrico.
Explicado así parece un proceso largo, pero en realidad está muy afinado. Las plantas industriales trabajan de forma continua, con bastante precisión. Eso sí, hay un punto que genera debate: las emisiones de óxidos de nitrógeno. No son precisamente inocuas. Por eso, muchas instalaciones están incorporando sistemas para reducir ese impacto.
Usos reales: donde entra en juego
Aquí es donde el ácido nítrico deja de ser teoría y pasa a lo práctico. Y lo cierto es que aparece en más sectores de los que uno pensaría.
Agricultura: probablemente el uso más evidente
Gran parte del ácido nítrico producido se destina a fertilizantes. Sobre todo, a la fabricación de nitrato de amonio. El motivo es sencillo: aporta nitrógeno. Y el nitrógeno es esencial para el crecimiento de las plantas. Sin él, los cultivos no rinden. En agricultura intensiva, por ejemplo, este tipo de fertilizantes marca la diferencia. 
Explosivos: necesarios, pero delicado
Otra aplicación importante, aunque menos cómoda de mencionar. Se usa en la fabricación de nitroglicerina y otros explosivos tipo TNT. En estos procesos, introduce grupos nitro en compuestos orgánicos. Eso cambia completamente su comportamiento. De repente, una sustancia relativamente estable se vuelve altamente energética. Estos usos están muy regulados, como es lógico. Pero siguen siendo fundamentales en sectores como la minería o determinadas obras civiles.
Metales: limpieza, protección y precisión
En metalurgia tiene varias funciones interesantes. Por ejemplo, se utiliza para limpiar superficies metálicas, eliminando óxidos y residuos. Esto es clave antes de ciertos tratamientos. También se emplea para pasivar acero inoxidable. Básicamente, crea una capa protectora que mejora su resistencia a la corrosión. Y luego está el grabado químico. En piezas de precisión, donde necesitas eliminar material de forma controlada, el ácido nítrico resulta bastante útil.
Electrónica: más presente de lo que parece
Aunque no se sabe mucho de ello, también tiene su papel en electrónica. En la fabricación de circuitos impresos o componentes, se utilizan ácidos para tratar superficies. El ácido nítrico es uno de ellos. Por ejemplo, para eliminar capas muy finas de metal durante la producción. Aquí la precisión es clave, y este tipo de compuestos lo permite.
No todo es ventaja: riesgos reales
A estas alturas ya queda claro que es un producto útil. Pero también hay que hablar de su lado menos amable. El ácido nítrico es peligroso. Puede causar quemaduras graves en la piel. En los ojos, el daño puede ser inmediato. Y sus vapores no son precisamente inofensivos: irritan las vías respiratorias y pueden provocar problemas más graves si la exposición es alta. Además, es muy reactivo. Puede reaccionar con materiales orgánicos o metales de forma violenta. En ciertas condiciones, eso implica calor, gases tóxicos… incluso explosiones.
Y mal gestionado… puede dar problemas serios. Al final, como pasa con tantas cosas en química, todo depende de cómo se usa.
Lecturas recomendadas
Temas:
- Química