La inteligencia artificial ya “escucha” los tumores y promete diagnósticos más rápidos y baratos
Un estudio liderado desde España explica cómo la IA puede identificar qué células forman un cáncer sin necesidad de microscopio ni bisturí
Comprar barato ya no siempre es comprar mal y los auriculares lo demuestran
Esto no es un vídeo: así es la Tierra en directo desde la Estación Espacial Internacional

La inteligencia artificial vuelve a colarse en uno de los terrenos más sensibles de la medicina, el diagnóstico del cáncer. Un nuevo estudio coordinado desde la Universidad Francisco de Vitoria muestra cómo los algoritmos ya son capaces de deducir la composición celular de un tumor a partir de datos moleculares, sin necesidad de microscopio ni análisis célula a célula. Un avance que apunta a diagnósticos más rápidos, personalizados y mucho más asumibles en costes.
Por qué saber qué células hay en un tumor es clave
Cada año se diagnostican en España cerca de 300.000 nuevos casos de cáncer. En muchos de ellos, conocer exactamente qué tipos de células forman el tumor es determinante para elegir el tratamiento más eficaz. No todos los tumores son iguales, ni responden de la misma forma a la quimioterapia, la inmunoterapia o los tratamientos dirigidos.
Hasta ahora, obtener esa información requería técnicas muy precisas y costosas, como el análisis célula a célula o el estudio histológico tradicional. Son métodos muy fiables, pero también lentos, caros y dependientes de especialistas muy cualificados. En algunos casos, el coste puede superar los 2.000 dólares por muestra.
El problema de analizar una “sopa” celular
Ahí es donde entra en juego la inteligencia artificial aplicada al cáncer. Es una alternativa más rápida y económica llamada bulk RNA-seq, una técnica que permite analizar qué genes están activos en una muestra de tejido. El problema es que ofrece una media global de todo el conjunto, sin distinguir qué tipo de célula ha expresado cada gen. Es como probar una sopa sin saber exactamente qué ingredientes lleva. Ahí es donde entra en juego uno de los grandes retos de la medicina personalizada actual, descifrar esa mezcla y entender qué células componen realmente un tejido tumoral.
Qué es la deconvolución celular con inteligencia artificial
La solución pasa por la llamada deconvolución celular. En lugar de separar físicamente cada célula, los algoritmos analizan la mezcla de datos y deducen qué proporción corresponde a cada tipo celular. El estudio lo compara con el trabajo de un sumiller capaz de identificar sabores en una mezcla compleja.
Gracias al deep learning, un tipo de inteligencia artificial especializada en detectar patrones muy sutiles en grandes volúmenes de datos, estos modelos pueden entrenarse con ejemplos conocidos y luego aplicarse a nuevas muestras. El resultado es una especie de radiografía digital del tejido, capaz de indicar cuántas células tumorales hay, cuántas defensas del sistema inmune están presentes o qué nivel de inflamación existe, todo sin intervenir directamente en el tejido.
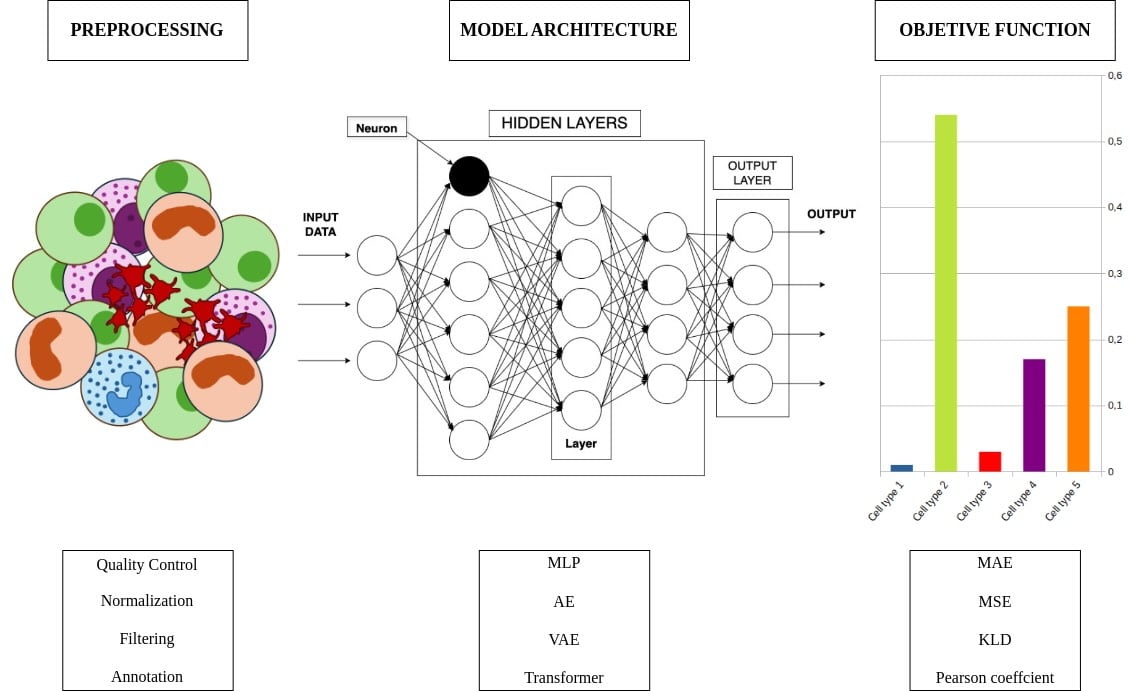
Un mapa completo de esta nueva disciplina
El equipo investigador ha realizado una revisión sistemática de la literatura científica para poner orden en un campo que crece muy rápido. De más de 170 estudios iniciales, solo 13 cumplían los criterios de rigor necesarios, como el uso de datos reales y revisión por pares.
El análisis muestra que la mayoría de modelos actuales se basan en redes neuronales relativamente sencillas, pero eficaces. También empiezan a aparecer enfoques más avanzados, como autoencoders o redes generativas, que ayudan a entrenar mejor los algoritmos cuando hay pocos datos disponibles. Curiosamente, tecnologías tan de moda como los transformers aún no se han aplicado en este ámbito, aunque los expertos creen que podrían marcar un punto de inflexión cuando lo hagan.
El gran reto antes de llegar al hospital
Uno de los principales obstáculos detectados es la falta de estándares comunes. Cada grupo de investigación procesa los datos de forma distinta y utiliza métricas diferentes para evaluar la precisión de sus modelos. Esto dificulta la comparación entre herramientas y retrasa su adopción clínica.
Para que esta tecnología llegue a los hospitales, los investigadores subrayan la necesidad de datos abiertos, modelos más transparentes y validaciones clínicas sólidas. No basta con que un algoritmo acierte: también debe explicar cómo llega a sus conclusiones para que los médicos puedan confiar en él.
Diagnósticos más rápidos, personalizados y asequibles
Si estos retos se superan, el impacto puede ser enorme. Los médicos podrían recibir, junto al informe tradicional, un panel digital que indique en minutos la composición exacta de un tumor. Esto permitiría ajustar mejor los tratamientos, monitorizar recaídas con análisis menos invasivos e incluso reducir costes al evitar pruebas complejas. La inteligencia artificial aplicada al cáncer comienza a ser una realidad.
Una revolución silenciosa que recuerda a otros grandes saltos impulsados por la inteligencia artificial en biomedicina. Escuchar los tejidos antes de cortar podría convertirse en una práctica habitual y cambiar para siempre la forma en que entendemos y combatimos el cáncer desde dentro.
Temas:
- Inteligencia artificial









