PH significado: qué es, cómo se mide y por qué es importante en química, biología y en la vida cotidiana
PH significado: descubre qué es el pH, cómo se mide y por qué es importante en química, biología y vida cotidiana.
Un pH corporal saludable
Crear un indicador de ph casero
Alcalinizar el agua en casa

El pH es un concepto fundamental en química, biología y en muchos aspectos de la vida cotidiana. Su relevancia radica en su capacidad para influir en procesos químicos, biológicos e industriales, así como en la salud humana y el medio ambiente.
Definición de pH y su significado
El término pH proviene del latín potentia hydrogenii, que significa “potencial de hidrógeno”. Es una medida que indica la acidez o alcalinidad de una solución acuosa. El pH se determina por la concentración de iones de hidrógeno presentes en esta.
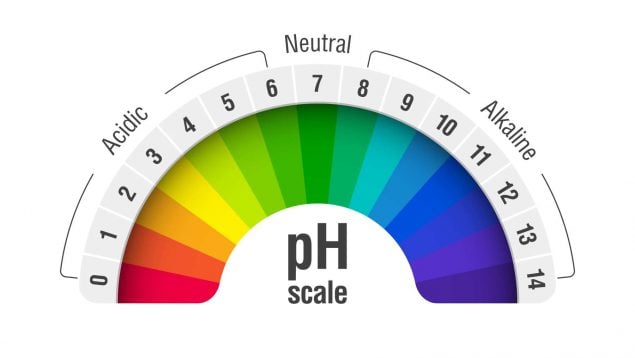
La escala de pH varía de 0 a 14:
- pH < 7. La solución es ácida. Cuanto menor es el valor, mayor es la acidez.
- pH = 7. La solución es neutra.
- pH > 7. La solución es alcalina o básica. Cuanto mayor es el valor, mayor es la alcalinidad.

Cómo se mide el pH: métodos y herramientas
La medición del pH es un proceso relativamente sencillo gracias a las herramientas modernas. Los métodos más comunes son los siguientes:
- Indicadores químicos. Sustancias como el papel tornasol, la fenolftaleína o el rojo de metilo cambian de color según el pH de la solución. Son económicos y fáciles de usar, pero menos precisos.
- Medidores de pH electrónicos (pH-metros). Son dispositivos que miden el pH con gran precisión mediante un electrodo sensible a los iones de hidrógeno.
- Tiras reactivas de pH. Contienen indicadores químicos que cambian de color al entrar en contacto con una solución. Debe compararse el color resultante con una escala de referencia para estimar el pH.
La elección del método depende del contexto. En un laboratorio se usa un pH-metro, mientras que en casa una tira reactiva suele ser suficiente.
Importancia del pH en la vida diaria
El pH está presente en varios aspectos de la vida cotidiana. Por ejemplo, los productos cosméticos, como champús y cremas, tienen un pH específico para que sean compatibles con la piel y el cabello. Un pH inadecuado puede causar irritación o sequedad.
El pH también afecta el sabor, la conservación y la seguridad de los alimentos. Por ejemplo, los alimentos enlatados suelen tener un pH bajo para evitar el crecimiento de bacterias.
Así mismo, se debe mantener un pH adecuado en las piscinas (7.2-7.8) para asegurar la eficacia de los desinfectantes. En los acuarios, el pH es vital para la salud de los peces.
El pH del suelo influye en la disponibilidad de nutrientes para las plantas, en agricultura. Un suelo demasiado ácido o alcalino limita el crecimiento de los vegetales.
pH en química y biología: ejemplos prácticos
En química, el pH es un factor determinante en las reacciones químicas y en la estabilidad de compuestos. Por ejemplo, en la síntesis de medicamentos, un pH incorrecto puede alterar la estructura de los compuestos o reducir su eficacia.
En biología, el pH regula procesos clave como los siguientes:
- Enzimas. Las enzimas, que catalizan las reacciones bioquímicas funcionan óptimamente en un rango de pH específico. Por ejemplo, la pepsina, una enzima del estómago, trabaja mejor en un pH muy ácido.
- Sangre humana. El pH de la sangre debe mantenerse entre 7,35 y 7,45. Pequeñas desviaciones pueden causar acidosis o alcalosis, afectando los órganos vitales.
- Ecosistemas acuáticos. Los organismos marinos, como corales y moluscos, dependen de un pH oceánico estable (alrededor de 8,1).
Consecuencias de un pH fuera del rango normal
Un pH desequilibrado tiene efectos perjudiciales en diferentes contextos. En el cuerpo humano, un pH sanguíneo fuera del rango normal puede causar trastornos graves.
De igual manera, la lluvia ácida, con un pH menor a 5,6, daña los ecosistemas, acidifica los suelos y los cuerpos de agua, y afecta la vida vegetal y animal. Muchas especies no toleran un pH bajo.
Así mismo, un pH inadecuado en procesos industriales puede reducir la calidad de los productos o dañar loa equipos. En la agricultura, un suelo con pH extremo limita la absorción de nutrientes, afectando el rendimiento.
Cómo mejorar el pH
Comer con más equilibrio
La alimentación es clave. No hace falta demonizar los alimentos ácidos ni vivir solo a base de ensaladas, pero sí conviene compensar. Las carnes rojas, los ultraprocesados, los refrescos azucarados o el alcohol tienden a dejar un “residuo ácido” que el cuerpo debe neutralizar.
En cambio, frutas como el plátano, el limón o la sandía, verduras de hoja verde y frutos secos crudos tienen un efecto más alcalinizante. Una regla sencilla es llenar medio plato con vegetales en cada comida y dejar los procesados para ocasiones puntuales.
Beber agua de forma constante
Parece un consejo básico, pero muchas veces lo olvidamos. El agua es la gran aliada de los riñones, que son los encargados de eliminar el exceso de ácidos. Si no bebemos lo suficiente, el cuerpo tiene que esforzarse más. Entre litro y medio y dos litros al día suele ser lo adecuado, aunque depende de la persona, el clima y la actividad física.
Respirar mejor
El pH no se regula solo por lo que comemos: también los pulmones tienen mucho que decir. Al exhalar eliminamos dióxido de carbono, y cuando hay demasiado, la sangre se vuelve más ácida. Por eso, prácticas como la respiración profunda, el yoga o simplemente caminar al aire libre pueden marcar la diferencia.
Movernos más
El ejercicio ayuda a oxigenar el cuerpo y a eliminar residuos ácidos. No hace falta convertirse en atleta: caminar media hora, montar en bici o bailar son opciones perfectas. Lo importante es la regularidad, no la intensidad.
Lecturas recomendadas
Temas:
- Química










