Tabla periódica: guía esencial de los elementos químicos
Tabla periódica: elementos, grupos, propiedades y curiosidades de la base de la química moderna. Toma nota de estos datos.
¿Cómo leer la tabla periódica?
Tablas periódicas más interesantes de la historia
Cambios en la tabla periódica
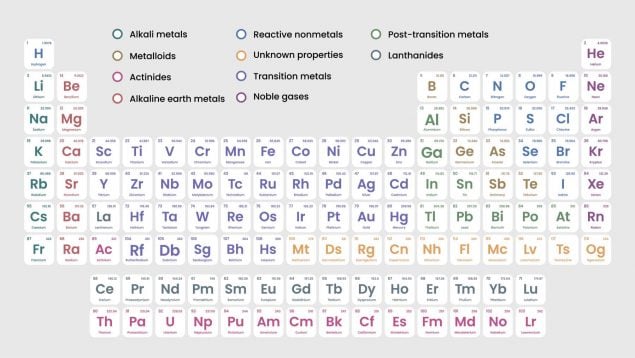

La tabla periódica es una obra maestra de la ciencia que organiza los bloques fundamentales de la materia: los elementos químicos. Esta tabla clasifica los componentes básicos del universo y es fundamental en la comprensión de la química, la física y la tecnología.
Orígenes de la Tabla Periódica
La idea de organizar los elementos químicos surgió en el siglo XIX, cuando los científicos comenzaron a identificar patrones en sus propiedades. Fue el químico ruso Dmitri Mendeléyev quien, en 1869, creó la primera versión ampliamente aceptada de la tabla periódica.
Organizó los elementos conocidos de acuerdo con su masa atómica y observó que sus propiedades se repetían de manera regular. A partir de esa observación formuló la ley periódica, que incluso le permitió predecir la existencia de elementos que todavía no se habían descubierto, como el galio y el germanio. Con el paso del tiempo y el avance del conocimiento, la tabla fue modificándose hasta basarse en el número atómico, que corresponde a la cantidad de protones en el núcleo de cada átomo.
Mendeléyev organizó los 63 elementos conocidos en ese momento según su peso atómico y propiedades químicas. Como hemos visto, dejó espacios vacíos para los elementos aún no descubiertos, como el galio y el germanio, que predijo con impresionante precisión.
La genialidad de Mendeléyev radicaba en su visión de la periodicidad. Detectó que las propiedades químicas y físicas de los elementos se repiten de manera predecible al aumentar el número atómico. Esta idea sentó las bases para la tabla moderna.
Estructura de la Tabla Periódica
La tabla periódica actual organiza los 118 elementos conocidos en un formato de filas y columnas. Sus componentes clave son los siguientes:
- Filas (períodos). Las siete filas horizontales representan los niveles de energía de los electrones en los átomos.
- Columnas (grupos). Las 18 columnas verticales agrupan elementos con propiedades químicas similares, a partir de configuraciones electrónicas análogas.
- Bloques. La tabla se divide en bloques (s, p, d, f) según el tipo de orbital electrónico ocupado por los electrones de valencia.
- Propiedades periódicas. La tabla revela tendencias claras, como el aumento del radio atómico hacia la izquierda y abajo, o la mayor electronegatividad hacia la derecha y arriba.
Cada elemento se representa con un símbolo químico, un número atómico (protones en el núcleo) y una masa atómica. Por ejemplo, el carbono (C) tiene un número atómico de 6 y una masa atómica promedio de 12.011 u.
Importancia de la Tabla periódica
La tabla periódica es una herramienta universal que tiene aplicaciones en diferentes campos. En Química, guía la predicción de las reacciones químicas, la formación de compuestos y el diseño de materiales. Por ejemplo, la reactividad de los halógenos (grupo 17) con los metales alcalinos (grupo 1) explica la formación de sales como el cloruro de sodio (NaCl).
También proporciona información sobre la estructura atómica y las propiedades nucleares, lo cual es esencial en la física nuclear y la investigación de partículas.
Los elementos como el carbono, el hidrógeno, el oxígeno y el nitrógeno son fundamentales para las moléculas de la vida. Otros, como el yodo o el hierro, son esenciales para los procesos biológicos.
La tabla es fundamental en el desarrollo de materiales avanzados, como los semiconductores (silicio, germanio) en electrónica, o los catalizadores (platino, paladio) en la industria automotriz. Los elementos de tierras raras, como el neodimio, son determinantes para elaborar los imanes en las turbinas eólicas y los dispositivos electrónicos.
Elementos y descubrimientos recientes
Actualmente, la tabla periódica incluye 118 elementos. Va desde el hidrógeno (Z=1) hasta el oganesson (Z=118). Los últimos elementos incluidos son el nihonio, el moscovio, el tenesino y el oganesson. Estos fueron confirmados oficialmente en 2016 por la Unión Internacional de Química Pura y Aplicada (IUPAC).
Esos elementos superpesados son sintéticos. Fueron creados en los laboratorios mediante colisiones de partículas. Tienen vidas extremadamente cortas en promedio, por lo cual son difíciles de estudiar.
La búsqueda de nuevos elementos continúa. Hay investigaciones enfocadas en el concepto de la “isla de estabilidad”; esta es una región teórica donde los elementos superpesados podrían tener vidas más largas. Laboratorios como el JINR en Rusia y el RIKEN en Japón lideran estas investigaciones, utilizando aceleradores de partículas.
La tabla periódica seguirá evolucionando. Los avances en química computacional y simulaciones cuánticas están permitiendo predecir las propiedades de elementos que aún no están sintetizados. Así mismo, la exploración espacial podría revelar nuevos elementos en otros planetas o estrellas.
Conclusión
Actualmente, la tabla periódica más que una lista ordenada, es un mapa del mundo químico: una guía que revela cómo está hecha la materia y cómo se enlazan las leyes que la gobiernan.
Gracias a ella, los científicos pueden comprender cómo se comportan los elementos, cómo se combinan y por qué la materia tiene las propiedades que la caracterizan. Desde su aparición en el siglo XIX, se ha convertido en una guía fundamental para la química, la física y muchas otras ciencias.
Lecturas recomendadas
Temas:
- Química









